|
|
|
|
|
|
Para más información sobre cada apartado hacer click en:
|
Key words: Cuvier's Beaked Whale, description, size, variation.
Descripción Cetáceo de tamaño medio. Su cabeza no es tan alargada como el género Mesoplodon ni tampoco evidencia un melón tan bulboso como Hyperoodon o Berardius (Heyning, 1989b). Presentan dos surcos en la cabeza en posición ventral que convergen anteriormente sin llegar a unirse y que se expanden durante el proceso de succión en la alimentación (ver Alimentación). Presenta una aleta dorsal falcada muy retrasada ubicada aproximadamente en los 2/3 de la longitud total, en la región lumbar, sus aletas pectorales son pequeñas y encajan en pequeñas depresiones laterales (Heyning, 1989b). Posee una pequeña concavidad en la parte superior de la cabeza. Su aleta caudal es ancha y no presenta ninguna muesca de separación entre los dos lóbulos. La mandíbula inferior se extiende por delante de la superior y el perfil de la boca está curvado hacia arriba. Ambos sexos presentan dos dientes en el extremo apical, uno en cada hemimandíbula que asoman externamente en los machos, aún con la mandíbula cerrada, y más raramente en las hembras, que miden hasta 60 mm de longitud. Hay dientes vestigiales en las encías en número de 24–26 de 13 mm de largo y 2 mm de diámetro a cada lado de la mandíbula superior y 31–33 a cada lado de la mandíbula inferior (Fraser, 1936; Gomerćić et al., 2006). Machos de color gris oscuro; el patrón de coloración es variable en hembras (Heyning, 1989b), pudiendo presentar colores grises y marrones en diferentes tonalidades, aclarándose hacia la posición ventral. Los juveniles suelen presentar una coloración muy oscura. Con la edad, la cabeza se vuelve más clara, casi blanca, especialmente en los machos (Heyning, 2002). Es frecuente la presencia de cicatrices en la piel en forma de dos surcos paralelos con pocos centímetros de distancia entre ellos provocados por los dientes de la mandíbula inferior de otros ejemplares de la misma especie y manchas claras circulares sin un patrón definido. Estas cicatrices son especialmente significativas en machos adultos en la región frontal debido a las luchas entre ellos. Presenta un vértex muy elevado que se superpone a los pasajes nasales externos, alargamiento de los senos pterigoideos (Heyning 1989b), los huesos nasales se presentan altamente desarrollados anterioposteriormente y las crestas premaxilares están expandidas transversalmente. Entre las crestas premaxilares y los nasales se abre un espacio cubierto por cartílago al que se unen los ligamentos que controlan la apertura del espiráculo (Heyning, 1989a). La familia Ziphiidae, junto con las familias Physeteridae y Kogiidae, presenta la mayor asimetría craneal de todos los vertebrados con hipertrofia del lado derecho asociada a la producción de sonidos múltiples de diferentes frecuencias simultáneamente (Heyning, 1989a; Cranford, 2008). El dimorfismo sexual en el ballenato de Cuvier se muestra en el desarrollo de un rostro más corto, más ancho y más denso en machos que hembras. La osificación mesorrostral es un carácter de dimorfismo sexual presente en los machos de la familia de los zifios y que consiste en el mayor desarrollo del vómer y en la osificación del cartílago mesorrostral (Heyning, 1989b), y aunque sus posibles funciones han sido ampliamente discutidas, la hipótesis ampliamente aceptada consistiría en un mayor fortalecimiento del rostro que protege frente a las embestidas de las luchas intraespecíficas de los machos (Heyning, 1984; MacLeod, 2002). En el ballenato de Cuvier, la osificación mesorrostral se produce en la mitad distal del canal mesorrostral, favoreciendo el desarrollo de una mayor profundidad en la concavidad prenasal (Mead y Fordyce, 2009; Heyning, 1989a), provocada por la reabsorción de la fosa premaxilar (Heyning, 1989a) o por la compresión del melón sobre la fosa premaxilar (Cranford 2008). El propio melón varía en forma y en posición con la edad. En los ejemplares adultos podemos considerar dos áreas bien diferenciadas que varían en densidad, la menos densa se trata de una estructura análoga aunque no homóloga al órgano spermaceti de los cachalotes (Heyning, 1989a), emplazada en la concavidad prenasal y que ha sido propuesta como melón funcional (McKenna, 2005), mientras que el área más densa se encuentra sobre la superficie dorsal de la primera y está rodeada por un extenso tejido conectivo.
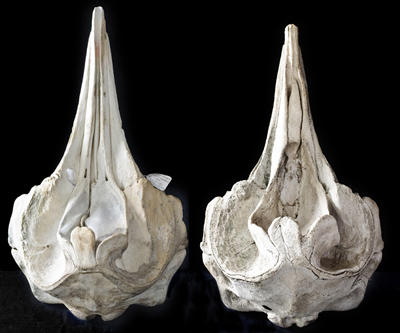
Figura 1. Vista dorsal del cráneo de adultos de Z. cavirostris. Izquierda, hembra (SGHN MA0749) y derecha, macho (SGHN MA0910). Museo da Natureza de la Sociedade Galega de Historia Natural. (C) I. Miján
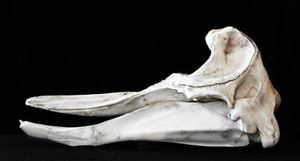
Figura 2. Vista lateral del cráneo de una hembra adulta de Z. cavirostris (SGHN MA0749). Museo da Natureza de la Sociedade Galega de Historia Natural. (C) I. Miján
Tamaño La longitud corporal media es de 6,13 m sin diferencias apreciables entre sexos, pudiendo alcanzar los 7 m (Heyning, 1989b).
Masa corporal La masa corporal puede alcanzar los 2.952,5 kg (Robineau y Di Natale, 1995).
Bioacústica La asimetría craneal juega un papel importante en la producción y emisión de sonidos para la ecolocalización, a lo que debemos sumar las estructuras óseas paquiosteoscleróticas de las áreas faciales que actúan como reflectores sonoros (Cranford et al., 2008), y los músculos rostrales que permiten, a su vez, variar la fisionomía del melón para focalizar los sonidos direccionalmente (Soldevilla et al., 2005). Se han observado dichos cambios en la morfología del melón en ejemplares en libertad con movimientos de derecha a izquierda y viceversa a modo de escaneo durante la producción de ultrasonidos de ecolocalización. Este patrón de escaneo se vuelve más intenso a partir de los 200 m de profundidad (Frantzis et al., 2002).
Variación geográfica Un análisis filogeográfico utilizando ADN mitocondrial ha revelado que hay un elevado aislamiento y poco flujo de genes entre océanos. Las poblaciones del Mediterráneo están diferenciadas de las del Atlántico (Dalebout et al., 2005).
Referencias Cranford, T. W., McKenna, M. F., Soldevilla, M. S., Wiggins, S. M., Goldbogen, J. A., Shadwick, R. E., Krysl, P., Leger, J. A., Hidebrand, J. A. (2008). Anatomic geometry of sound transmission and reception in Cuvier’s beaked whale (Ziphius cavirostris). The Anatomical Record, 291: 353-378 Dalebout, M. L., Robertson, K. M., Frantzis, A., Engelhaupt, D., Mignucci-Giannoni, A. A., Rosario-Delestre, R. J., Baker, C. S. (2005). Worldwide structure of mtDNA diversity among Cuvier's beaked whales (Ziphius cavirostris): implications for threatened populations. Molecular Ecology, 14 (11): 3353-3371. Frantzis, A., Goold, J. C., Skarsoulis, E. K., Taroudakis, M. I., Kandia, V. (2002). Clicks from Cuvier’s beaked whales, Ziphius Cavirostris. The Journal of the Acoustical Society of America,112 (1):34-37. Fraser, F. C. (1936). Vestigial teeth in specimens of Cuvier's Whale (Ziphius cavirostris) stranded on the Scottish coast. Scot. Nat., 1936: 153-157. Gomerćić, H., Gomerćić, M.D., Gomerćić, T., Lucić, H., Dalebout, M., Galov, A., Surković, D. Ćkrtić, S., Vuković, S., Huber, D. (2006). Biological aspects of Cuvier's beaked whale (Ziphius cavirostris) recorded in the Croatian part of the Adriatic Sea. European Journal for Wildlife Research, 52: 182-187. Heyning J. E. (1984). Functional morphology envolved in intra-specific fighting of the beaked whale, Mesoplodon carlhubbsi. Canadian Journal of Zoology, 62: 1645-1654. Heyning J. E. (1989a). Comparative facial Anatomy of Beaked Whales (Ziphiidae) and a Systematic Revision among the Families of Extant Odontoceti. Nat. Hist. Mus. Los Angeles County Contributions in Science. 405: 1-64. Heyning J. E. (1989b). Cuvier’s beaked whale, Ziphius cavirsotris. Pp. 289-308. En: Ridgway, S. H., Harrison, R. (Eds.). Handbook of marine mammals. Vol. 4. River dolphins and larger toothed whales. Academic Press, London. Heyning J. E. (2002). Cuvier’s beaked whale (Ziphius cavirostris). Pp. 305-307. En: Perrin, W.F., Würsig, B., Thewissen, J. G. M. (Eds.). Encyclopedia of marine mammals. Academic Press, London. McKenna M. F. (2005). Comparative morphology of the odontocete melon: functional and evolutionary interpretations. M. Sc. Thesis. San Diego State University. MacLeod C. D. (2002). Possible functions of the ultradense bone in the rostrum of Blainville’s beaked whale (Mesoplodon densirostris). Canadian Journal of Zoology, 80: 178-184 Mead J. G., Fordyce, R. E. (2009). The Therian Skull. A Lexicon with Emphasis on the Odontocetes. Smithsonian Contributions to Zoology, 627. Robineau, D., Di Natale, A. (1995). Ziphius cavirostris G. Cuvier, 1823 – Schnabelwal. Pp. 526-543. En: Robineau, D., Duguy, R., Klima, M. (Eds.). Band 6: Meeressäuger. Teil I: Whale und Delphine – Cetacea. Teil I B: Ziphiidae, Kogiidae, Physeteridae, Balaenidae, Balaenopteridae. En: Niethammer, J., Krapp, F. (Eds.). Handbuch der Säugetiere Europas. Aula Verlag, Wiesbaden. Soldevilla, M. S., McKenna, M. F., Wiggins, S. M., Shadwick, R. E., Crandford, T. W., Hildebrand, J. A. (2005). Cuvier’s beaked whale (Ziphius cavirostris) head tissues: physical properties an CT imaging. The Journal of Experimental Biology, 208: 2319-2332.
Ismael Miján Fecha de publicación: 4-02-2011 Miján, I. (2017). Ballenato de Cuvier – Ziphius cavirostris. En: Enciclopedia Virtual de los Vertebrados Españoles. Salvador, A., Barja, I. (Eds.). Museo Nacional de Ciencias Naturales, Madrid. http://www.vertebradosibericos.org/
|
|
|
|
|
|
|